表面自由エネルギーとは?
表面自由エネルギーとは何か?
液体に分子間力による表面張力が存在するのと同じように、固体にも分子間力によってその表面積を小さくしようとする力が存在しています。この固体に働く表面張力のことを「表面自由エネルギー(Surface Free Energy, SFE)」と呼びます。
表面自由エネルギーの単位は、表面張力と同様に[mN/m](または[mJ/m2])で表され、値の大小はその固体が持つ、別の液体や固体に対する濡れやすさを意味します。簡単なイメージとして、「固体の表面自由エネルギーが小さい=液体が濡れにくい」、「固体の表面自由エネルギーが大きい=液体が濡れやすい」と考えらえます。身近な例を挙げると、非常に低い表面自由エネルギーを持つフッ素樹脂(PTFEなど)をフライパンにコーティングすることで汚れが付着しづらい加工が行われています。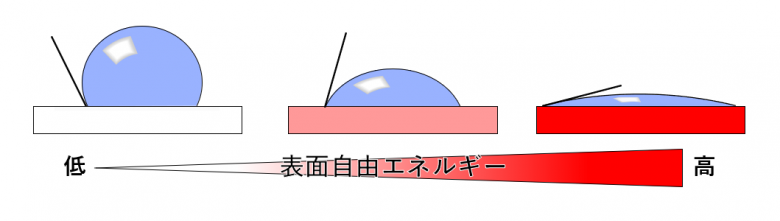
表面自由エネルギーは、表面張力と同様に、固体が持つ分子間力の成分の和で構成されます。
分子間力は分散力、配向力、誘起力、水素結合力に分類され、それぞれ分散成分、極性成分、誘起成分、水素結合成分として表面自由エネルギーを構成します。
| 分子間力 | 表面自由エネルギーの成分 | 概要 |
| 分散力 | 分散成分(dispersion, σd) | すべての分子間に生じる瞬間的な電荷の偏りにより生じる力。 |
| 配向力 | 極性成分(polar, σp) | 極性分子間で生じる電荷の偏りによって生じる力。 |
| 誘起力 | 誘起成分(induction, σi) | 極性分子が無極性分子に双極子を誘起することで生じる力。 |
| 水素結合 | 水素結合成分(hydrogen, σh) | 電気陰性度が大きな原子が、極性の強い水素原子を引き付ける力。 O-HやF-Hなど。 |
これら成分のうち、誘起成分は非常に弱いことから無視することができ、水素結合成分はしばしば極性成分内にまとめられます。
下記は液体ですがいくつかの試薬の表面張力とそれを構成する分散成分と極性成分を記載したものです。※文献により異なります。
水: 表面張力72.8mN/m(分散成分21.8mN/m+極性成分51.0mN/m)
ホルムアミド: 表面張力58.2mN/m(分散成分39.5mN/m+極性成18.7mN/m)
ジヨードメタン: 表面張力50.8mN/m(分散成分50.8mN/m+極性成分0mN/m)
n-ヘキサデカン: 表面張力27.6mN/m(分散成分27.6mN/m+極性成分0mN/m)
なぜ表面自由エネルギーを評価するのか?
濡れ性を定量化できる接触角ですが、Youngの式が示すように、その値は「液体の表面張力、固体の表面自由エネルギー、液体と固体の界面張力」によって決定されます。つまり、液体と固体の単独の濡れ性だけではなく、液体と固体の相性によっても影響を受けます。
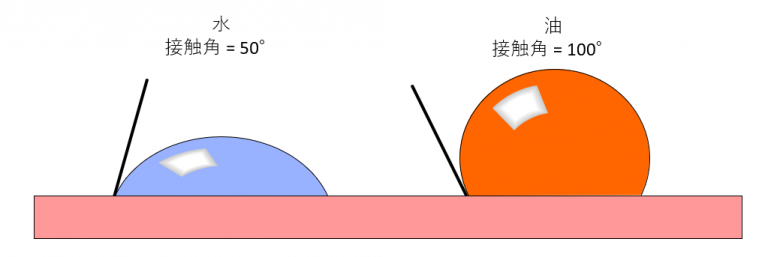
例えば、表面張力が高い(濡れ広がりにくいはずの)液体である水の接触角が50°と高い濡れ性を示すある固体に対して、表面張力が低い(濡れ広がりやすいはずの)液体である油の接触角が100°と低い濡れ性を示す場合があります。これは、その固体表面が、極性成分が多く含まれる水とはなじみやすく、分散成分が多く含まれる油とはなじみにくい性質を持っていることが理由です。
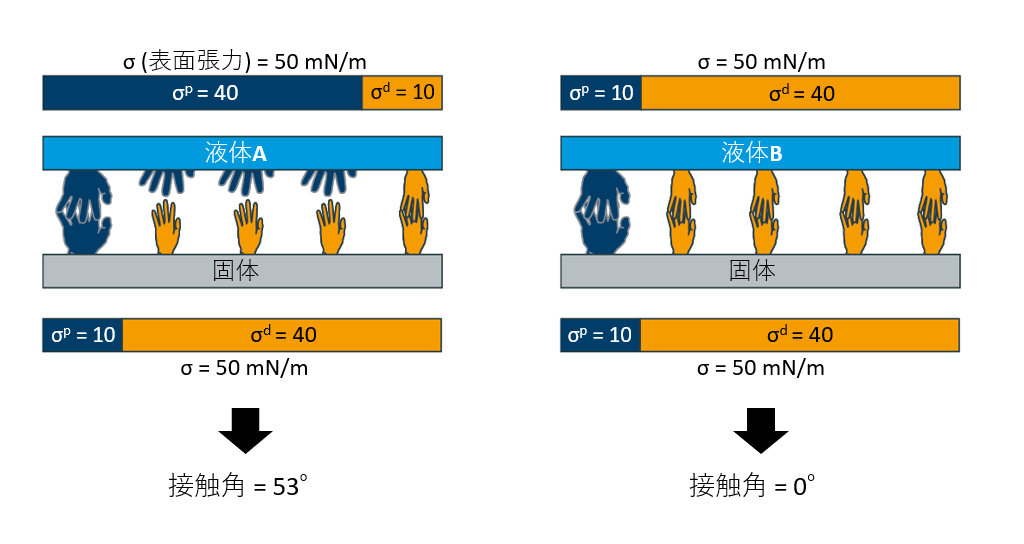
表面張力も表面自由エネルギーも分散成分と極性成分に切り分けることができますが、これら成分の比率が近しいほど固体/液体間の界面張力が低くなる(なじみが良くなる)ことが知られています。
例えば、表面張力が同じ50mN/mである液体A(極性成分40mN/m+分散成分10mN/m)と液体B(極性成分10mN/m+分散成分40mN/m)の液滴を、表面自由エネルギーが50mN/mである固体(極性成分10mN/m+分散成分40mN/m)に滴下して接触角を測定した際、成分比率が異なる液体Aは53°を示し、成分比率が同じ液体Bは0°を示します。このように、液体と固体の表面張力値が同じでも、その成分比率の違いは濡れ性に差をもたらします。
いわば、接触角は液体と固体の相性によって決まる相対値、表面自由エネルギーは固体自体の濡れ性を示す絶対値と言えます。
固体の表面自由エネルギーとそれを構成する各成分を解析することにより、その固体表面がどのような物性になっているのか、また、その固体に対してどのような液体が高い/低い濡れ性を示すのかを予想することが可能になります。
表面自由エネルギーの測定方法と解析理論
液体の表面張力はプレート法やペンダントドロップ法で測定することができますが、流動性を持たない固体の表面自由エネルギーを直接測定する方法はありません。
そこで、物性が既知の液体試薬2種類以上を使用して、その固体の接触角を測定し、液体の物性値と接触角の測定値から計算によって表面自由エネルギーを算出します。
表面自由エネルギーを求める理論は多数存在しており、分散成分と極性成分に切り分けるものや、さらに極性成分内の水素結合エネルギーまでを切り分けるものなどもあります。
下記は代表的な理論式です。
| 解析理論 | 計算式 | 表面自由エネルギーの構成成分 |
| OWRK (Owens-Wendt -Rable-Kaelble) |
分散成分(σd)+極性成分(σp) | |
| Fowkes (フォークス) |
分散成分と非分散成分 | |
| Extended Fowkes (拡張フォークス) |
分散成分(σd)+極性成分(σp)+水素結合エネルギー(σh) | |
| Acid-Base (酸―塩基、Oss, Good) |
ルイス塩基+ルイス酸 | |
| Zisman | 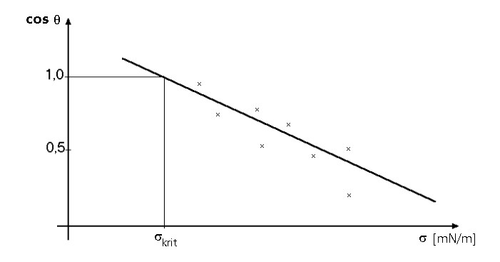 |
固体の臨界表面張力(成分分けなし) |
| EoS (Equation of State) |
成分分けなし | |
| Wu | 分散成分(σd)+極性成分(σp) | |
| Schultz 1 | - | 分散成分(σd)+極性成分(σp) |
理論式は多数ありますが、一般的にはOWRK法などがよく使用されています。
OWRK法はFowkes法を基に編み出された解析理論であり、必要な試薬の数は2種類で、その試薬に求められる条件が少ないなどの特徴があります。
接触角による算出以外にも、濡れ試薬(ダインペン、テストインク)を用いて評価する方法もあります。
表面張力が段階的に異なる液体を固体表面に塗布し、どの表面張力値の液体までが濡れたかを目視で判断することによって固体の表面自由エネルギーを評価します。
表面自由エネルギーの活用事例
- 表面洗浄の評価(固体表面の清浄性が十分に高まっているかどうか)
- 表面処理の確認(プラズマ処理やコロナ処理が十分に行われているかどうか)
- 接着剤の最適化(対象の固体に対してどのような液体の接着剤を設計すれば接着性が向上するか)









